Gás Ideal ou Perfeito – Lei Geral
Chama-se gás ideal, ou perfeito, um modelo de gás cujas moléculas (de volume desprezível) se movem ao acaso, todas com mesma velocidade média, se chocam elasticamente entre si e com as paredes do recipiente, além de não exercerem ações mútuas (exceto quando colidem).
Para os gases perfeitos, ou ideais, a pressão $p$, o volume $V$ e a temperatura absoluta $T$ obedecem à chamada Lei Geral dos Gases Perfeitos que relacionam dois estados quaisquer da massa gasosa:
$$\displaystyle \frac{p_1 \cdot V_1}{T_1}=\frac{p_2 \cdot V_2}{T_2}$$
Chama-se gás ideal, ou perfeito, um modelo de gás cujas moléculas (de volume desprezível) se movem ao acaso, todas com mesma velocidade média, se chocam elasticamente entre si e com as paredes do recipiente, além de não exercerem ações mútuas (exceto quando colidem).
Para os gases perfeitos, ou ideais, a pressão $p$, o volume $V$ e a temperatura absoluta $T$ obedecem à chamada Lei Geral dos Gases Perfeitos que relacionam dois estados quaisquer da massa gasosa:
$$\displaystyle \frac{p_1 \cdot V_1}{T_1}=\frac{p_2 \cdot V_2}{T_2}$$
Transformação Isobárica
Na transformação isobárica, a pressão permanece constante $\left ( p_1=p_2 \right )$, valendo a expressão:
Na transformação isobárica, a pressão permanece constante $\left ( p_1=p_2 \right )$, valendo a expressão:
$\displaystyle \frac{V_1}{T_1}= \frac{V_2}{T_2}$
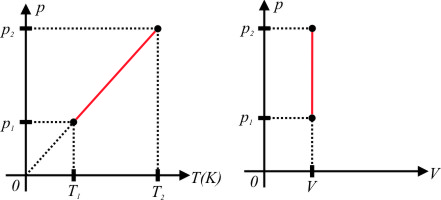
As representações gráficas são as seguintes:
[Figura 1]
Na transformação isocórica o volume permanece constante $\left ( V_1=V_2 \right )$, valendo a fórmula:
$\displaystyle \frac{p_1}{T_1}= \frac{p_2}{T_2}$
Segue abaixo as representações gráficas:
[Figura 2]
Aplicações
1) Um gás ideal sofre uma transformação isobárica na qual o volume aumenta de $20 cm^3$ para $50cm^3$. Sendo a temperatura inicial igual a $27^\circ C$. Determinar a temperatura final do gás, em $^\circ C.
Temos que:
$V_1=20cm^3$
$V_2=50cm^3$
$t_1=27^\circ C$
$V_2=50cm^3$
$t_1=27^\circ C$
Na fórmula de transformação isobárica, $\frac{V_1}{T_1}= \frac{V_2}{T_2}$, as temperaturas devem ser expressas em kelvin $\left ( K \right )$.
Assim:
$T_1=t_1+273$
$T_1=27+273$
$T_1=300K$
Substituindo na fórmula:
Como a resposta deve ser dada em Celsius, fazemos:
2) O gráfico representa a transformação isocórica de um gás ideal. Determinar a pressão do gás no estado final $B$.
$\displaystyle \frac{20}{300}= \frac{50}{T_2}$
$\displaystyle T_2=\frac{50 \cdot300}{20}$
$T_2=750K$
Como a resposta deve ser dada em Celsius, fazemos:
$t_2=T_2-273$
$t_2=750-273$
$t_2=477^\circ C$
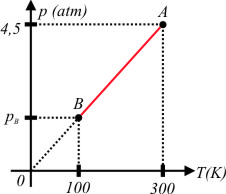
2) O gráfico representa a transformação isocórica de um gás ideal. Determinar a pressão do gás no estado final $B$.
Do gráfico, obtemos os valores:
$P_A=4,5atm$
$t-A=300K$
$T_B=100K$
Aplicando a fórmula da transformação isocórica:
$\displaystyle \frac{p_A}{T_A}= \frac{p_B}{T_B}$
$\displaystyle \frac{4,5}{300}= \frac{p_B}{100}$
$\displaystyle p_B=\frac{4,5 \cdot 100}{300}$
$p_B=1,5atm$
Transformação Isotérmica
Na transformação isotérmica, a temperatura permanece constante $\left ( T_1=T_2 \right )$, valendo a expressão da Lei de Boyle-Mariotte:
$\displaystyle p_1V_1=p_2V_2$
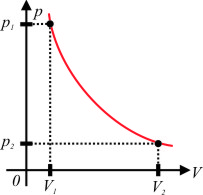
Graficamente, no diagrama $p\times V$ a transformação isotérmica é representada pela curva denominada hipérbole equilátera:
[Figura 4]
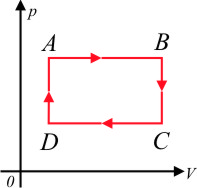
Transformação Cíclica
As transformações isobárica, isocórica e isotérmica são transformações abertas, pois o estado final não coincide com o estado inicial. A transformação é dita fechada ou cíclica (ciclo) quando o estado final coincide com o inicial. Na figura 5 é representada graficamente um ciclo, onde $A$ é o estado inicial e também o estado final do gás:
Aplicações:
3) A pressão de um gás ideal aumenta de $10N/m^2$ para $30N/m^2$. Admitindo que a temperatura do gás permaneça constante durante o processo, determinar a relação entre o volume final e o volume inicial do gás.
Como a temperatura permanece constante, a transformação é isotérmica, valendo a Lei de Boyle-Mariotte: $p_1V1=p_2V_2$. Temos que:
$\displaystyle p_1=10N/m^2$
$\displaystyle p_2=30N/m^2$
Assim:
$\displaystyle 10 \cdot V_1=30 \cdot V_2$
$\displaystyle \frac{V_2}{V_1}=\frac{10}{30}$
$\displaystyle \frac{V_2}{V_1}=\frac{1}{3}$
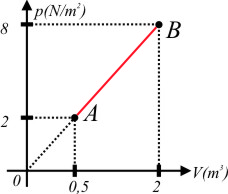
4) O gráfico abaixo indica uma transformação gasosa $AB$ de um gás perfeito, cuja temperatura inicial é de $200K$. Determinar a temperatura final do gás.
[Figura 6]
Como há modificação das três grandezas, pressão, volume e temperatura, devemos aplicar a lei geral dos gases:
$\displaystyle \frac{p_AV_A}{T_A}=\frac{p_BV_B}{T_B}$
Temos que:
$T_A=200K$
e do gráfico obtemos que:
$p_A=2N/m^2$
$p_B=8N/m^2$
$V_A=0,5m^3$
Substituindo na fórmula, obtemos:
$\displaystyle \frac{2 \cdot 0,5}{200}=\frac{8 \cdot 2}{T_B}$
$\displaystyle T_B=\frac{8 \cdot 2 \cdot 200}{2 \cdot 0,5}$
$T_B=3.200K$
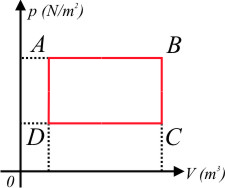
5) Certa massa de gás ideal realiza a transformação cíclica $ABCDA$ indicada na figura abaixo. Sendo $200K$ a temperatura no estado $A$, determine a temperatura dos demais estados do gás.
A transformação AB é isobárica, então:
$\frac{V_A}{T_A}=\frac{V_B}{T_B} \left\{\begin{matrix} V_A=0,2m^3\\ V_B=0,6m^3\\ T_A=200K\\ \end{matrix}\right.$
$\displaystyle \frac{0,2}{200}=\frac{0,6}{T_B}$
$T_B=600K$
A transformação $BC$ é isocórica, então:
$\frac{p_B}{T_B}=\frac{p_C}{T_C} \left\{\begin{matrix} p_B=4N/m^2\\ p_C=2N/m^2\\ T_B=600K\\ \end{matrix}\right.$
$\displaystyle \frac{4}{600}=\frac{2}{T_C}$
$T_C=300K$
A transformação $CD$ é isobárica, então:
$\frac{V_C}{T_C}=\frac{V_D}{T_D}\left \{\begin{matrix} V_C=0,6m^3\\ V_D=0,2m^3\\ T_C=300K\\ \end{matrix}\right.$
$\displaystyle \frac{0,6}{300}=\frac{0,2}{T_D}$
$T_D=100K$




ficou uma ótima explicação ... me salvou eespero q teenha salvo o seu sálario tbm!
ResponderExcluirAgradeço seu comentário, amigo. Volte sempre.
ResponderExcluirCara, essa explicação é muito boa, estou estudando para a segunda fase da UFBA e este conteúdo me ajudou bem.
ResponderExcluirObrigado, parabéns.
Obrigado Jesiel. Bons estudos!
ResponderExcluirMuitíssimo obrigada!
ResponderExcluirMe ajudou bastante ao entendimento. *o*
Explicação muito boa!! *o*
gostei
ResponderExcluirmuito obrigada
Perfeito. Mas pra mim faltou a transformação adiabática. Tenho alguma dificuldade com ela.
ResponderExcluir